1. Sự điện phân
Sự điện phân là quá trình oxi hóa khử xảy ra ở bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li. Như vậy, sự điện phân là quá trình sử đụng diện năng để tạo ra sự biến đổi hóa học.
2. Điện phân nóng chảy
- Thường điện phân muối clorua của kim loại mạnh, bazơ của kim loại kiềm, hoặc oxit nhôm (muối Halogen, Bazơ, Oxit nhôm)
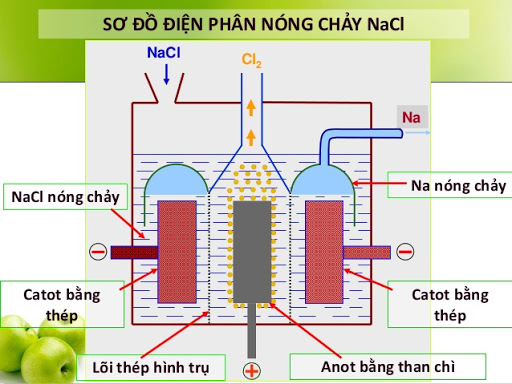
3. Điện phân dung dịch
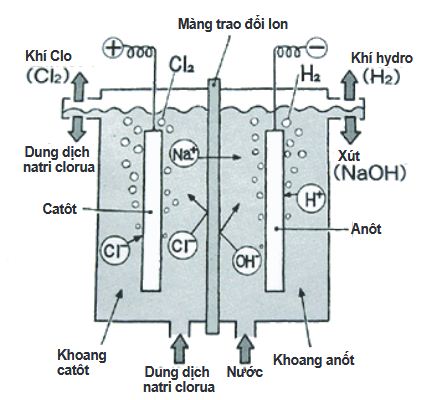
a. Muối của kim loại tan
- Điện phân dung dịch muối halogenua ( gốc –Cl, -Br …) có màng ngăn, tạo bazơ + halogen + H2
- Điện phân dung dịch muối halogen nếu không có màng ngăn, Cl2 sinh ra phản ứng với dung dịch kiềm tạo nước giaven.
b. Muối của kim loại trung bình yếu: khi điện phân dung dịch sinh kim loại
- Nếu muối chứa gốc halogenua ( gốc –Cl, - Br …): Sản phẩm là KL + phi kim
- Nếu muối chứa gốc có oxi: Sản phẩm là KL + Axit + O2
- Muối của kim loại tan với gốc axit có oxi, axit có oxi, bazơ tan như NaNO3, NaOH, H2SO4
4. Ứng dụng của sự điện phân
Sự điện phân có nhiều ứng dụng trong công nghiệp
a. Điều chế các kim loại
Một số kim loại, dù có thế điện cực chuẩn âm nhưng vẫn có thể điều chế bằng cách điện phân dung dịch muối của chúng.
Thí dụ: hơn 50% sản lượng Zn của thế giới được điều chế bằng phương pháp điện phân dung dịch ZnSO4.
Những kim loại có thế điện cực chuẩn rất âm như các kim loại kiềm (Na, K...) được điều chế bằng cách điện phân những hợp chất ion của chúng ở dạng nóng chảy.
b. Điều chế một số phi kim như H2, O2, F2, Cl2
c. Điều chế một số hợp chất như KMnO4, NaOH, H2O2, nước Gia-ven...
d. Tinh chế một số kim loại như Cu, Pb, Zn, Fe, Ag, Au...
e. Mạ điện: điện phân với anot tan cũng được dùng trong kĩ thuật mạ điện, nhằm bảo vệ kim loại khỏi bị ăn mòn và tạo vẻ đẹp cho vật mạ. Trong mạ điện, anot là kim loại dùng để mạ như Cu, Ag, Au, Cr, Ni.... catot là vật cần mạ. Lớp mạ thường rất mỏng có độ dày từ 5.10-5 đến 1.10-3 cm.

.jpg)
.jpg)




.jpg)
.jpg)




















