I. BẠC
Bạc là kim loại chuyển tiếp ở chu kì 5, nhóm IB.
Trong các hợp chất, bạc có số oxi hóa phổ biến là +1.
1. Tính chất của bạc.
- Bạc là kim loại nặng, tonc = 960,5oC, có màu trắng, dẫn điện và dẫn nhiệt tốt nhất.
- Bạc không bị oxi hóa trong không khí ở bất kì nhiệt độ nào. Nó tác dụng với axit có tính oxi hóa mạnh như HNO3, H2SO4 đặc nóng.
Ag + 2HNO3 → AgNO3+ NO2 + H2O
- Bạc có màu đen khi tiếp xúc với nước hoặc không khí ẩm có chứa H2S:
4Ag + 2H2S + O2 → 2Ag2S↓ (đen) + 2H2O
2. Ứng dụng của bạc
- Bạc tinh khiết dùng để chế tác đồ trang sức, vật trang trí, mạ bạc, chế tạo các linh kiện kĩ thuật trong vô tuyến.
- Chế tạo một số hợp kim có tính chất rất quý như hợp kim Ag - Cu, Ag - Au được dùng để chế tác đồ trang sức, đúc tiền, ...
- Ion Ag+ có khả năng sát trùng, diệt khuẩn.
3. Trạng thái tự nhiên
- Trong tự nhiên, bạc có ở trạng thái tự do, nhưng phần lớn ở dạng hợp chất lẫn trong quặng đồng, quặng chì.
- Bạc được điều chế chủ yếu từ các hợp chất cùng với đồng và chì.
II. VÀNG
Vàng là kim loại chuyển tiếp ở chu kì 6, nhóm IB.
Trong các hợp chất, vàng có số oxi hóa phổ biến là +3.
1. Tính chất của vàng
- Vàng là kim loại mềm, màu vàng, dẻo, có tính dẫn điện, dẫn nhiệt tốt (sau Ag và Cu).
- Vàng có tính khử yếu nhất so với các kim loại khác. Không bị oxi hóa trong không khí kể cả ở nhiệt độ cao. Không bị hòa tan trong các axit có tính oxi hóa, chỉ bị hòa tan trong nước cường toan (đó là dung dịch hỗn hợp gồm 1 thể tích HNO3 đặc và 3 thể tích HCl đặc):
Au + HNO3 + 3HCl → AuCl3 + 2H2O + NO
- Vàng tan trong dung dịch xianua của kim loại kiềm do tạo thành ion phức [Au(CN)2].
2. Ứng dụng của vàng
- Chế tạo đồ trang sức.
- Mạ vàng cho các đồ trang sức.
- Chế tạo hợp kim quý.
III. NIKEN
Niken là kim loại chuyển tiếp nằm ở ô số 28, thuộc chu kì 4, nhóm VIIIB.
Trong các hợp chất, niken có số oxi hóa phổ biến là +2, ngoài ra còn có số oxi hóa +3.
1. Tính chất của Ni
- Ni là kim loại màu trắng bạc, rất cứng, khối lượng riêng lớn (D = 8,9g/cm3), tonc = 1455oC.
- Ni có tính khử yếu hơn sắt, không tác dụng được với nước và oxi không khí ở nhiệt độ thường. Không tác dụng với axit thường do trên bề mặt có lớp oxit bảo vệ. Niken dễ dàng tan trong dung dịch axit HNO3 đặc nóng
- Tác dụng được với nhiều đơn chất và hợp chất, nhưng không tác dụng được với H2
2. Ứng dụng của Ni
Niken được dùng để chế tạo hợp kim chống ăn mòn và chịu nhiệt cao. Chẳng hạn như:
- Hợp kim Inva Ni - Fe có hệ số giãn nở rất nhỏ, được dùng trong kĩ thuật vô tuyến, replay nhiệt.
- Hợp kim Cu - Ni có tính bền vững cao, không bị nước biển ăn mòn, được dùng để đúc chân vịt tàu biển, tuabin cho động cơ máy bay.
Ngoài ra, một phần Ni được dùng trong kĩ thuật mạ điện, chế tạo ắc - quy.
- Trong công nghiệp hóa chất thì Ni được dùng chất xúc tác. Hơn 80% lượng Ni được sản xuất dùng trong ngành luyện kim, thép chứa Ni có độ bền cao về mặt hóa học và cơ học.
IV. KẼM
Kẽm là kim loại chuyển tiếp nằm ở ô số 30, chu kì 4, nhóm IIB.
Trong các hợp chất, kẽm có số oxi hóa là +2.
1. Tính chất của kẽm
- Zn là kim loại có màu lam nhạt. Trong không khí ẩm, kẽm bị phủ một lớp oxit mỏng nên có màu xám. Kẽm là kim loại có khối lượng riêng lớn (D = 7,13g/cm3), có tonc = 419,5oC.
- Ở điều kiện thường, Zn khá giòn nên không kéo dài được, nhưng khi đun nóng từ 100 - 150oC lại dẻo và dai, đến 200oC thì giòn trở lại và có thể tán được thành bột.
- Zn ở trạng thái rắn và các hợp chất của kẽm không độc. Riêng hơi của ZnO thì rất độc.
- Zn là một kim loại khá hoạt động, có tính khử mạnh hơn sắt. Phản ứng với nhiều phi kim như O2, Cl2, S, ...
2. Ứng dụng của kẽm
- Mạ (hoặc tráng) để bảo vệ bề mặt các dụng cụ, thiết bị bằng sắt, thép để chống gỉ, chống ăn mòn.
- Chế tạo hợp kim như hợp kim với Cu - Zn.
- Chế tạo pin điện hóa, phổ biến nhất là pin Zn - Mn ...
- Một số hợp chất của Zn dùng trong y học, chẳng hạn như ZnO dùng làm thuốc giảm đau dây thần kinh, chữa bệnh eczema, bệnh ngứa, ...
V. THIẾC
- Thiếc nằm ở ô số 50, thuộc nhóm IVA, chu kì 5 trong bảng tuần hoàn.
- Trong hợp chất, thiết có số oxi hóa là +2 và +4, trong đó số oxi hóa phổ biến và bền hơn là +2.
1. Tính chất của thiếc
- Kim loại màu trắng, dẻo, dễ cán mỏng.
- Nhiệt độ nóng chảy 232oC, nhiệt độ sôi 2620oC.
- Có 2 dạng: thiếc trắng và thiếc xám.
- Là kim loại có tính khử yếu:
+ Bị oxi hóa ở nhiệt độ cao.
+ Tác dụng chậm với dung dịch HCl và H2SO4 loãng tạo Sn (II) và khí H2.
Với dung dịch HNO3 loãng tạo thành muối Sn (II) nhưng không giải phóng H2.
Với HNO3 đặc và H2SO4 đặc tạo Sn (IV)
+ Tan trong kiềm đặc: NaOH, KOH.
Ví dụ:
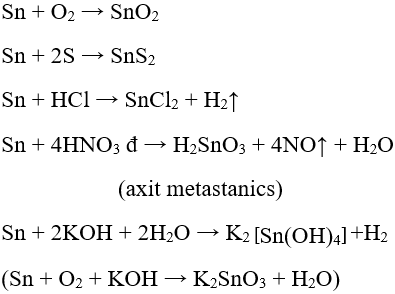
2. Ứng dụng của thiếc
- Một lượng lớn Sn dùng để phủ lên bề mặt của sắt để chống gỉ (sắt tây).
- Hợp kim Sn - Pb (nóng chảy ở 180oC) dùng để hàn.
- Dùng chế tạo các hợp kim có tính chịu ma sát, dùng để chế ổ trục quay.
VI. CHÌ
Chì nằm ở ô số 82, thuộc nhóm IVA, chu kì 6 trong bảng tuần hoàn.
Trong hợp chất, chì có số oxi hóa là +2 và +4, trong đó số oxi hóa phổ biến và bền hơn là +2.
1. Tính chất của chì
- Màu trắng hơi xanh, mềm, dễ dát mỏng và kéo sợi.
- Là kim loại nặng.
- Có tính khử yếu, không tác dụng với các dung dịch HCl và H2SO4. Tan nhanh trong dung dịch H2SO4 đặc nóng và tạo muối Pb(HSO4)2. Dễ tan trong HNO3, tan chậm trong HNO3 đặc.
![]()
- Tan chậm trong dung dịch kiềm nóng.
Pb + 2KOH → K2PbO2+ H2
- Chì và các hợp chất của chì đều rất độc. Một lượng chì vào cơ thể sẽ gây ra bệnh làm xám men răng và có thể gây rối loạn thần kinh.
2. Ứng dụng của chì
Chì được dùng để chế tạo các bản cực ắc quy, vỏ dây cáp, đầu đạn và dùng để chế tạo thiết bị để bảo vệ các tia phóng xạ. Ngoài ra, nó còn dùng để chế tạo các hợp kim.

.jpg)
.jpg)




.jpg)
.jpg)




















