Silic dioxit tuy có công thức phân tử giống với cacbon dioxit nhưng không tồn tại ở dạng từng phân tử riêng lẻ mà dưới dạng tinh thể, nghĩa là một phân tử khổng lồ. Ba dạng tinh thể của silic dioxit ở áp suất thường là thạch anh, tridimit và cristobalit. Mỗi một dạng đa hình này lại có hai dạng: dạng anpha bền ở nhiệt độ thấp và dạng beta bền ở nhiệt độ cao.

Tất cả những dạng tinh thể này đều bao gồm những nhóm tứ diện SiO4 nối với nhau qua những nguyên tử O chung. Trong tứ diện SiO4, nguyên tử Si nằm ở tâm của tứ diện liên kết cộng hóa trị với bốn nguyên tử O nằm ở các đỉnh của tứ diện. Như vậy, mỗi nguyên tử O liên kết với hai nguyên tử Si ở hai tứ diện khác nhau và tính trung bình cứ trên một nguyên tử Si có hai nguyên tử O và công thức kinh nghiệm của SiO2
Ba dạng đa hình của silic dioxit có cách sắp xếp khác nhau của các nhóm tứ diện SiO4 ở trong tinh thể. Trong thạch anh, những nhóm tứ diện được sắp xếp sao cho các nguyên tử Si nằm trên một đường xoắn ốc.
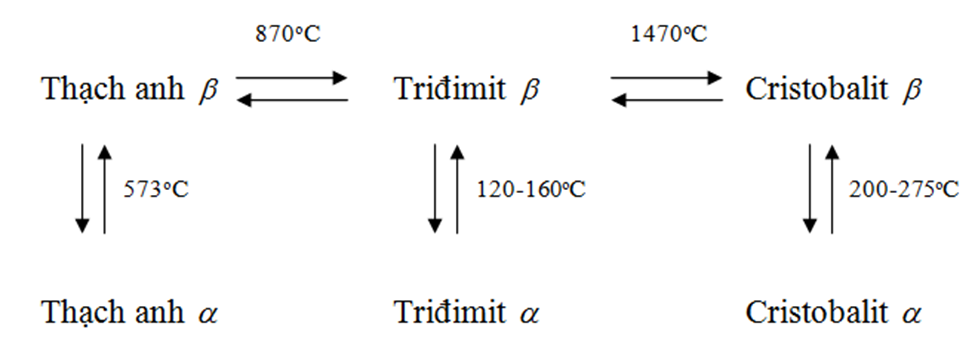
Tỉ khối của thạch anh là 2,56 của tridimit là 2,3 và của cristobalit là 2,2. Sự khác nhau giữa dạng anpha và dạng beta của mỗi dạng đa hình đó là do sự quay một ít của các tứ diện đối với nhau nhưng cách sắp xếp chung của các tứ diện không biến đổi. Do vậy, chúng ta có thể hiểu dễ dàng tại sao sự biến đổi giữa các dạng anpha và beta xảy ra nhanh chóng và ở nhiệt độ thấp hơn so với sự biến đổi từ dạng đa hình này sang dạng đa hình kia: trường hợp thứ nhất không đòi hỏi sự phá vỡ liên kết còn trường hợp thứ hai đòi hỏi sự phá vỡ và xây dựng lại tất cả các liên kết. Vì quá trình biến đổi dạng đa hình này sang dạng đa hình khác của silic dioxit xảy ra chậm và cần năng lượng hoạt hóa cao cho nên thạch anh, tridimit và cristobalit đều tồn tại ở trong thiên nhiên mặc dù ở nhiệt độ thường chỉ có thạch anh anpha là bền nhất và các dạng tinh thể khác chỉ là bền giả.
Ngoài ba dạng tinh thể đa hình trên, ở trong thiên nhiên còn có một số dạng khác nữa của silic dioxit có kiến trúc vi tinh thể. Một trong những dạng đó đã được sử dụng trong thực tế là mã não. Mã não là chất rắn, trong suốt, gồm có những vùng có màu sắc khác nhau và rất cứng. Mã não thường được dùng làm cối, chày để nghiền những vật liệu cứng và để làm đồ trang trí.
Opan là một loại đá quý không có kiến trúc tinh thể. Nó gồm những hạt cầu SiO2 liên kết với nhau tạo nên những lỗ trống chứa không khí, nước hay hơi nước. Do chứa các tạp chất, opan có các màu khác nhau: vàng, nâu, đỏ, lục và đen. Dạng mờ đục có màu trắng sữa nên khoáng vật này có tên gọi là opan.
Gần đây người ta chế tạo được hai dạng tinh thể mới của silic dioxit nặng hơn thạch anh là coesit vf stishovit. Hai dạng này về sau mới được phát hiện ở các thiên thạch.
Khi để nguội chậm silic dioxit đã nóng chảy hoặc khi đun nóng bất kì dạng nào của silic dioxit đến nhiệt độ hóa mềm, thu được một vật liệu vô định hình giống như thủy tinh. Những vật liệu dạng thủy tinh như vậy, về một mặt giống với chất rắn và về một số mặt khác giống với chất lỏng. Ở nhiệt độ khá thấp, chẳng hạn như ở nhiệt độ thường, vật liệu dạng thủy tinh tạo nên khối rắn có hình dạng xác định, đôi khi có độ bền cơ học cao, độ cứng lớn... Nhưng ở nhiệt độ cao hơn, vật liệu dạng thủy tinh có tính chất giống như một chất lỏng chậm đông có độ nhớt rất lớn. Khác với dạng tinh thể, chất dạng thủy tinh có tính đằng hướng và không nóng chảy ở nhiệt độ không đổi mà hóa mềm ở nhiệt độ thấp hơn nhiều so với khi chảy lỏng ra. Bằng phương pháp Ronghen, người ta xác định được rằng trong trạng thái thủy tinh, mỗi nguyên tử vẫn được bao quanh bởi những nguyên tử khác giống như trong trạng thái tinh thể nhưng những nguyên tử đó sắp xếp một cách hỗn loạn hơn. Một ví dụ cụ thể đã gặp trước đây là trường hợp của B2O3. Một số chất khác cũng cho trạng thái thủy tinh là: selen, lưu huỳnh dẻo, berili florua, silic dioxit, gecmani dioxit...

.jpg)
.jpg)




.jpg)
.jpg)




















