Thông tin chi tiết về phương trình
Điều kiện phản ứng khi cho tác dụng Cl2 + O2
- Chất xúc tác: không có
- Nhiệt độ: thường
- Áp suất: thường
- Điều kiện khác: không có
Quá trình phản ứng Cl2 + O2
Quá trình: Dẫn khí Cl2 vào lọ đựng khí O2 có nút đậy
Lưu ý: Khí oxi là một phi kim rất hoạt động, đặc biệt ở nhiệt độ cao, dễ dàng tham gia phản ứng hóa học với nhiều phi kim có tính khử như C, N2, P, S. Tuy nhiên, Cl2 có tính oxi hóa mạnh hơn oxi và không có tính khử nên không thể phản ứng với O2.
Hiện tượng xảy ra sau phản ứng Cl2 + O2
Hiện tượng: Phản ứng không xảy ra
Thông tin chi tiết các chất tham gia phản ứng
Thông tin về Cl2 (clo)
- Nguyên tử khối: 70.9060
- Màu sắc: Vàng lục nhạt
- Trạng thái: Thể khí

Clo là một chất khí có màu vàng lục, nặng hơn không khí và có mùi khó chịu. Clo được sử dụng chủ yếu làm chất tẩy trắng trong sản xuất giấy và vải để tạo ra nhiều loại sản phẩm. Bên cạnh đó, clo là một chất tẩy rửa và khử trùng gia đình được sử dụng phổ biến. ...
Thông tin về O2 (oxi)
- Nguyên tử khối: 31.99880 ± 0.00060
- Màu sắc: không màu
- Trạng thái: Chất khí

Oxy là một chất khí không màu, không mùi và không vị là một chất khí cần thiết cho sự tồn tại của con người. Oxy có nhiều ứng dụng trong ngành sản xuất thép và các quá trình luyện, chế tạo kim loại khác, trong hóa chất, dược phẩm, chế biến dầu khí, sản xuất thủy tinh và gốm cũng như sản xuất giấy và...
Thông tin chi tiết các chất sản phẩm sau phản ứng
Thông tin về Cl2O7 (Diclo heptoxit)
- Nguyên tử khối: 182.9018
- Màu sắc: chưa cập nhật
- Trạng thái: chưa cập nhật
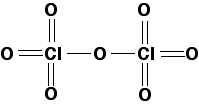
Diclo heptoxit là chất lỏng không màu, thủy phân sẽ tạo thành axit pecloric Diclo heptoxit được sản xuất bằng cách chưng cất axit pecloric với sự có mặt của chất khử nước là photpho pentoxit: 2 HClO4 + P4O10 → Cl2O7 + H2P4O11 Ngoài ra, điclo heptoxit còn được điều chế bằng cách nhiệt phân axit ...

.jpg)
.jpg)




.jpg)
.jpg)