A. KIẾN THỨC CẦN NẮM VỮNG
I. CẤU TẠO NGUYÊN TỬ VÀ PHÂN TỬ CỦA CÁC HALOGEN
- Bán kinh nguyên tử tăng dần từ flo đến iot
- Lớp ngoài cùng có 7 electron
- Phân tử gồm 2 nguyên tử, liên kết là cộng hóa trị không cực

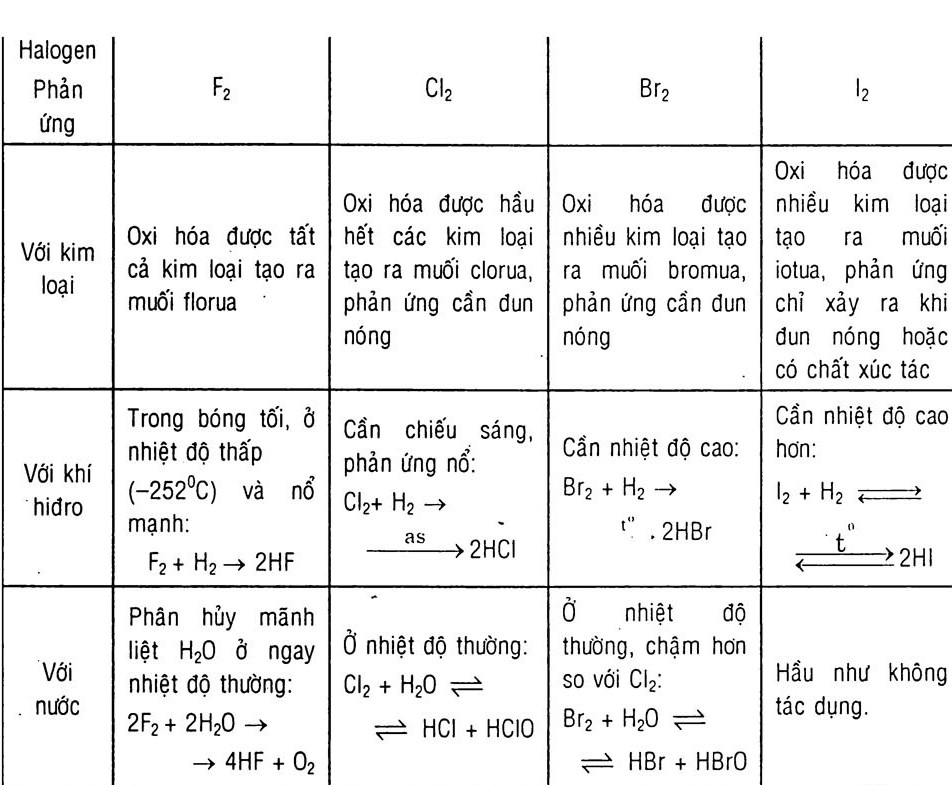
II. TÍNH CHẤT HÓA HỌC
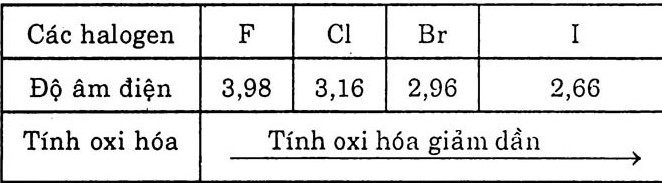
- Tính oxi hóa: Oxi hóa được hầu hết kim loại, nhiều phi kim và hợp chất
- Tính oxi hóa giảm dần từ flo đến iot
III. TÍNH CHẤT HÓA HỌC CỦA HỢP CHẤT HALOGEN
1. Axit halogenhdric
Dung dịch HF là axit yếu còn các dung dịch HCl, HBr, HI đều là các axit mạnh
2. Hợp chất có oxi
Nước Gia-ven và clorua vôi có tính tẩy màu và sát trùng do các muôi NaClO và CaOCl2 là các chất oxi hóa mạnh.
IV. PHƯƠNG PHÁP ĐIỀU CHẾ CÁC ĐƠN CHẤT HALOGEN

V. PHÂN BIỆT CÁC ION F- ; Cl- ; I-
Thuốc thử: AgNO3
NaF + AgNO3 → không p.ứ
NaCl + AgNO3 → AgCl + NaNO3
NaBr + AgNO3 → AgBr + NaNO3
NaI + AgNO3 → AgI + NaNO3

.jpg)
.jpg)




.jpg)
.jpg)




















