A. BENZEN VÀ ĐỒNG ĐẲNG
I. ĐỒNG ĐẲNG, ĐỒNG PHÂN, DANH PHÁP, CẤU TẠO
1. Dãy đồng đẳng của benzen
C6H6 (benzen), C7H8 (toluen), C8H10, ... , CnH2n-6 (n ≥ 6)
2. Đồng phân, danh pháp
Đồng phân
C6H6 và C7H8 không có đồng phân hidrocacbon thơm.
Từ C8H10 trở đi có:
Đồng phân vị trí tương đối của các nhóm ankyl
Đồng phân cấu tạo mạch cacbon của nhánh
Danh pháp
Tên hệ thống: nhóm ankyl + benzen
Chú ý: Nếu vòng benzen liên kết với nhiều nhóm ankyl tên gọi: số chỉ vị trí nhánh + tên nhánh + benzen
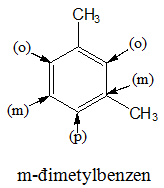
Cách đánh số các nguyên tử C trong vòng benzen sao cho tổng chỉ số trong tên gọi là nhỏ nhất.
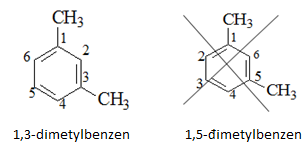
3. Cấu tạo
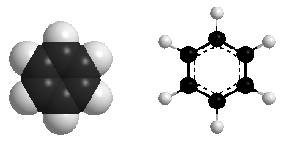
Mô hình benzen
Có 3 liên kết đôi, có cấu trúc lục giác đều.
Cả 6 nguyên tử C và 6 nguyên tử H cùng nằm trên một mặt phẳng.
Có hai cách biểu diễn công thức của benzen:
II. TÍNH CHẤT VẬT LÝ
Các hiđrocacbon thơm đều là chất lỏng hoặc rắn ở điều kiện thường ; chúng có nhiệt độ sôi tăng theo chiều tăng của phân tử khối.
Hiđrocacbon thơm ở thể lỏng có mùi đặc trưng, không tan trong nước, nhẹ hơn nước, hòa tan được nhiều chất hữu cơ.
III. TÍNH CHẤT HÓA HỌC
Benzen tương đối dễ tham gia phản ứng thế hơn so với các chất oxi hóa. Đó cũng chính là tính chất hóa học đặc trưng chung của các hiđrocacbon thơm nên được gọi là tính thơm
1. Thế nguyên tử H của vòng benzen
a) Phản ứng với halogen
Benzen phản ứng thế với brom:
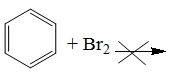
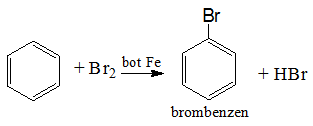
(ĐK: có xúc tác bột Fe)
Toluen tác dụng với brom:
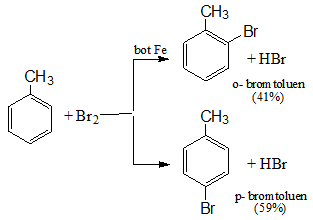
Phản ứng với axit nitric:
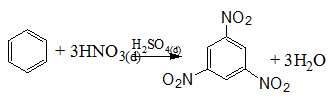
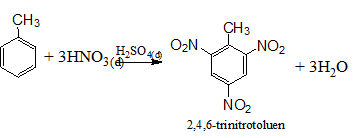
Quy tắc thế ở vòng benzen: khi ở vòng benzen đã có sẵn nhóm ankyl (hay các nhóm –OH, -NH2, -OCH3,...), phản ứng thế vào vòng sẽ dễ dàng hơn và ưu tiên thế vào vị trí o-, p-. Nếu vòng benzen đã có sẵn nhóm –NO2 ( hoặc các nhóm –COOH, -SO3H, ...) phản ứng thế vào vòng sẽ khó hơn và ưu tiên xảy ra ở vị trí m-.
b) Thế nguyên tử H của mạch nhánh
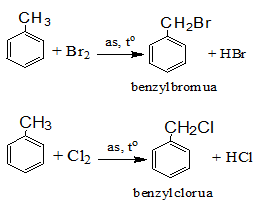
2. Phản ứng cộng
a) Cộng Hidro
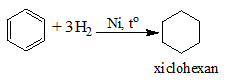
b) Cộng Clo
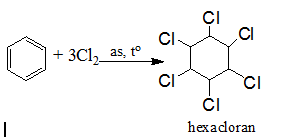
Chú ý: Phản ứng này được dùng để sản xuất thuốc trừ sâu 666 nhưng do chất này có độc tính cao và phân hủy chậm nên ngày nay không được sử dụng.
3. Phản ứng oxi hóa
a) Phản ứng oxi hóa không hoàn toàn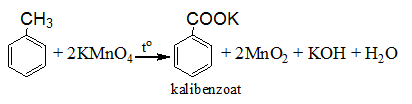
.png)
Khi đun nóng hai ống nghiệm trong nồi cách thủy:
Benzen vẫn không làm mất màu dung dịch KMnO4
Toluen làm mất màu dung dịch KMnO4 , tạo kết tủa MnO2

b) Phản ứng oxi hóa hoàn toàn
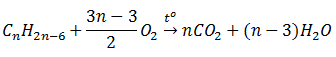
Nhận xét: Số mol CO2 luôn lớn hơn số mol H2O
B. MỘT SỐ HIDROCACBON THƠM KHÁC
I. STIREN
1. Cấu tạo và tính chất vật lí
a) Cấu tạo
Stiren có CTPT: C8H8
Công thức cấu tạo: 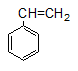
b) Tính chất vật lí
Stiren (còn gọi là Vinylbenzen) là chất lỏng, không màu, sôi ở 146oC, không tan trong nước nhưng tan nhiều trong dung môi hữu cơ.
2. Tính chất hóa học
Stiren có đặc điểm phần nhánh giống etilen, phần vòng giống benzen. Vì vậy, stiren thể hiện tính chất hóa học giống etilen ở phần mạch nhánh và thể hiện tính chất giống benzen ở phần nhân thơm.
a) Phản ứng với dung dịch brom và hidro
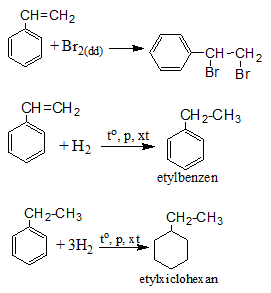
b) Phản ứng trùng hợp
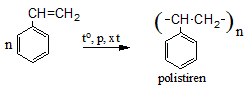
II. NAPHTALEN
1. Cấu tạo và tính chất vật lí
Công thức phân tử: C10H8
Công thức cấu tạo: 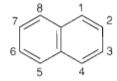
Naphtalen (băng phiến) là chất rắn, nóng chảy ở 80oC, tan trong benzen, ete, ... và có tính thăng hoa.
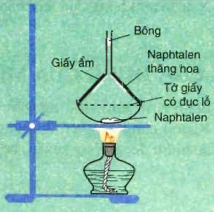
Thí nghiệm Naphtalen thăng hoa
2. Tính chất hóa học
a) Phản ứng thế
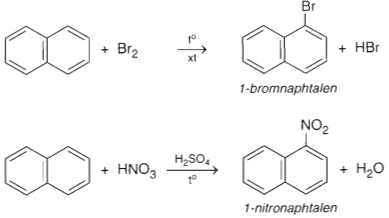
b) Phản ứng cộng
.png)
C. MỘT SỐ ỨNG DỤNG CỦA HIDROCACBON THƠM


.jpg)
.jpg)




.jpg)
.jpg)




















