A. ANĐEHIT
I. ĐỊNH NGHĨA, PHÂN LOẠI, DANH PHÁP
1. Định nghĩa
Là hợp chất hữu cơ phân tử có chứa nhóm –CH=O liên kết trực tiếp với gốc hidrocacbon hay nguyên tử H
Nhóm-CHO là nhóm chức của andehit, được gọi là nhóm cacbandehit.
Ví dụ: HCH=O,CH3CH=O
2. Phân loại
Dựa vào đặc điểm cấu tạo của gốc Hidrocacbon và số nhóm chức -CH=O chia thành:
Anđehit no, mạch hở, đơn chức như HCHO; CH3CHO,...Có công thức tổng quát: CnH2n+1CHO (x ≥ 0) hay CnH2nO (n ≥ 1)
Anđehit không no
Anđehit thơm
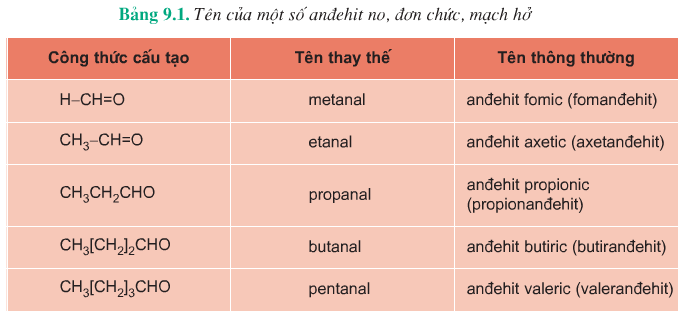
3. Danh pháp
Cách gọi tên Anđehit bằng tên thay thế:
Bước 1: Chọn mạch C dài nhất chứa nhóm -CHO làm mạch chính.
Bước 2: Đánh số từ Cacbon ở nhóm chức -CHO
Bước 3: Hidrocacbon tương ứng + al
II. ĐẶC ĐIỂM CẤU TẠO. TÍNH CHẤT VẬT LÝ
1. Đặc điểm cấu tạo
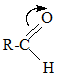
Liên kết C=O gồm 1 liên kết xích ma(σσ) bền và 1 liên kết pi (ππ) kém bền hơn ⇒ Có tính chất giống anken (tham gia phản ứng cộng, phản ứng oxi hóa)
2. Tính chất vật lí
HCHO, CH3CHO là chất khí, tan tốt trong nước, có nhiệt độ sôi thấp.
Các anđehit tiếp theo là chất lỏng hoặc chất rắn, độ tan trong nước giảm dần theo chiều tăng của phân tử khối.
Dung dịch nước của anđehit fomic được gọi là fomon. Dung dịch HCHO (37-40%) được gọi là fomalin.
Do anđehit không có liên kết H nên nhiệt độ sôi thấp hơn ancol tương ứng.
III. TÍNH CHẤT HÓA HỌC
1. Phản ứng cộng Hidro
CH3–CH=O + H2 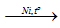 CH3 – CH2 – OH
CH3 – CH2 – OH
(anđehit axetic) (ancol etylic)
2. Phản ứng oxi hóa không hoàn toàn.
Các em tiến hành quan sát thí nghiệm tráng bạc của anđehit fomic sau:
Hiện tượng: Có kết tủa trắng. Khi ngâm dung dịch trong cốc nước nóng một thời gian thì thấy trên thành ống nghiệm có bám một lớp kim loại trắng sáng, có thể soi gương được.
Giải thích: HCHO + 2AgNO3 + H2O + 3NH3 → HCOONH4 + 2NH4NO3 + 2Ag↓
Nhận xét: Anđehit vừa thể hiện tính oxi hóa vừa thể hiện tính khử.
Khi bị khử, anđehit chuyển thành ancol bậc I tương ứng.
Khi bị oxi hóa, anđehit chuyển thành axit cacboxylic (hoặc muối của axit cacboxylic) tương ứng.
IV. ĐIỀU CHẾ
1. Từ ancol
R – CH2OH + CuO![]() R – CHO + Cu + H2O
R – CHO + Cu + H2O
Ví dụ: CH3–CH2OH + CuO ![]() CH3CHO + Cu + H2O
CH3CHO + Cu + H2O
2. Từ Hidrocacbon
Từ Metan: CH4 + O2 ![]() H-CH=O + H2O
H-CH=O + H2O
Từ Etilen: 2CH2 = CH2 + O2 ![]() 2 CH3 – CH=O
2 CH3 – CH=O
V. ỨNG DỤNG
Là nguyên liệu sản xuất nhựa phenol - formanđehit, nhựa urê - formanđehit
Nước của formanđehit (fomon) dùng để tẩy uế, làm chất sát trùng...
Anđehit axetic dùng sản xuất axit axetic làm nguyên liệu cho nhiều ngành sản xuất
B. XETON
I. ĐỊNH NGHĨA
Là hợp chất hữu cơ có chứa nhóm >C=O liên kết trực tiếp với 2 gốc hidrocacbon
Ví dụ: CH3COCH3 (đimetylxeton hoặc axeton), CH3COC6H5 (Metyl phenyl xeton hoặc axeton phenon)
II. TÍNH CHẤT HÓA HỌC
CH3–CO–CH3 + H2CH3–CH(OH)– CH3
Khác với anđehit, xeton không tham gia phản ứng tráng bạc.
III. ĐIỀU CHẾ
1. Từ ancol
R – CH(OH) – R’ + CuO![]() R – CO – R’ + Cu + H2O
R – CO – R’ + Cu + H2O
Ví dụ: CH3–CO–CH3 +CuO ![]() CH3–CHOH–CH3 + Cu+ H2O
CH3–CHOH–CH3 + Cu+ H2O
2. Từ Hidrocacbon
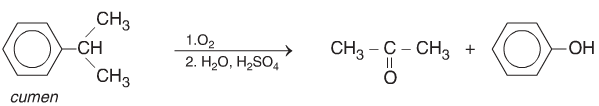
Oxi hóa không hoàn toàn Cumen thu được axeton và Phenol theo sơ đồ:
IV. ỨNG DỤNG
Axeton làm dung môi hoà tan được nhiều chất hữu cơ.

.jpg)
.jpg)




.jpg)
.jpg)




















