1. Cây cao su và nhựa cao su
Cao su thiên nhiên được lấy từ nhựa của một số loài cây, nhưng chủ yếu là cây hevea brasiliensis có nguồn gốc ở Braxin, được trồng nhiều ở Nam Mĩ, Châu Phi, Đông Nam Á trong đó có Việt Nam.
Để khai thác, người ta khía vỏ cây cao su thành rãnh xung quanh thân cây theo đường xoắn cho nhựa chảy ra rồi hứng lấy nhựa (còn gọi là mủ cao su hay latex). Trong nhựa cao su có khoảng 40% là chất rắn, trong đó có tới 90% là hợp chất cao phân tử của hidrocacbon không no, 10% là các thành phần khác như protein, lipit, gluxit, muối vô cơ...
Để sơ chế, làm đông tụ nhựa cao su, người ta cho axit axetic hay axit fomic vào, nhựa cao su đông tụ thành tảng, lấy ra hun sấy, thu được cao su thô hay cao su sống, gọi là crep.
Trong thiên nhiên còn một loại cây khác, là balata hay gutta-peccha, cũng lấy được từ vỏ cây chất có tính đàn hồi tương tự cao su gọi là gutta-peccha, nhưng khối lượng phân tử và cấu hình khác với phân tử cao su thiên nhiên.

Cây cao su và mủ cao su
2. Cấu trúc của cao su thiên nhiên
Cao su thiên nhiên có công thức nguyên là (C5H8)n.
Khi đun nóng cao su ở nhiệt độ khoảng 300oC, người ta thu được isopren. Ozon hóa cao su tạo thành ozonit rồi thủy phân cho một sản phẩm với hiệu suất tới 90% là andehit levulic .
Từ các dữ liệu trên có thể suy ra rằng cao su thiên nhiên là polime của isopren
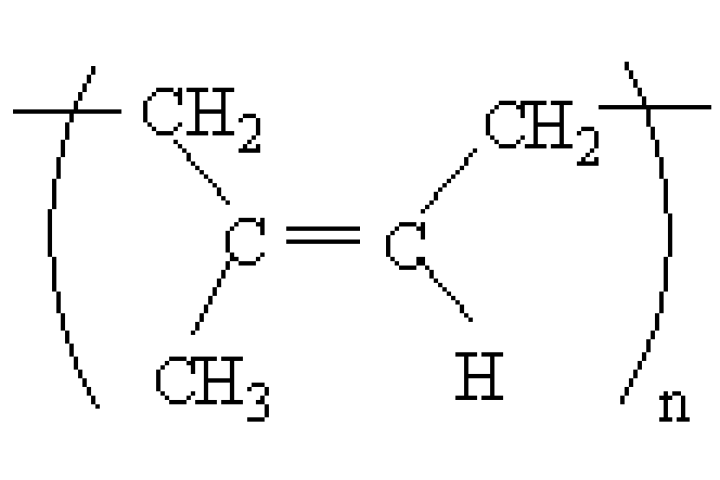
với n = 20.000
Trong mạch cao phân tử của cao su có cấu tạo lập thể điều hòa dạng cis, có thể biểu diễn như sau:
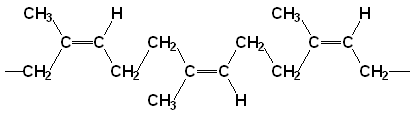
Còn gutta-peccha, có thành phần phân tử và hóa tính gần như đồng nhất với cao su nhưng hệ số trùng hợp n = 600 đến 700 và các mắt xích đều có cấu hình tran
3. Tính chất
Cao su có tính chất đặc biệt là tính đàn hồi, tức là tính có thể biến dạng khi có lực cơ học bên ngoài tác dụng vào (kéo, nén...) và trở lại dạng ban đầu khi lực thôi tác dụng.
Tính đàn hồi của cao su do cấu tạo của nó gây nên: trong phân tử polime của cao su còn có nhiều nối đôi, có cấu trúc mạch hình sợi với cấu hình cis ở các mắt xích. Bình thường các chuỗi polime xoắn lại hoặc cuộn lại. Khi kéo căng, các chuỗi đó duỗi ra làm sợi cao su dãn ra; khi ngừng kéo các chuỗi đó lại cuộn lại nên sợi cao su có xu hướng co về hình dạng ban đầu.
Ngoài ra, cao su còn có một số tính chất lí, hóa học khác nhau như: cao su không dẫn nhiệt và điện, không thấm khí và nước; cao su tan được trong một số hidrocacbon như benzen, xăng, dầu thông và trong một số dẫn xuất halogen như clorofom, nhưng không tan trong các dung môi phân cực như ancol, axeton, nước...
Phân tử polime của cao su còn nhiều nối đôi nên cao su hay bị lão hóa khi để lâu ngoài không khí, nhất là được xúc tiến khi đun nóng hay chiếu sáng... làm thay đổi tính chất cơ lí của cao su, làm giảm độ bền, vẻ đẹp.
Cũng do các liên kết đôi trong phân tử nên cao su còn có thể tham gia phản ứng với clo, HCl... tạo nên các dẫn xuất của cao su có nhiều ứng dụng trong thực tế. Chẳng hạn như:
- Cao su clo hóa: Là cao su thiên nhiên đã cho tác dụng với clo. Trong quá trình tương tác đã xảy ra phản ứng cộng clo vào liên kết đôi và cả phản ứng thế. Thành phần và cấu tạo của cao su clo hóa không cố định mà tùy thuộc vào điều kiện phản ứng. Tùy theo thành phần clo trong phân tử, tính chất của cao su clo hóa sẽ khác nhau: cao su có 40% clo thì mềm, còn cao su có chứa 65% clo lại rắn và bền hóa học. Cao su clo hóa được dùng trong việc chế sơn, vecni, thuốc vẽ. Sơn cao su rất bền, dùng để sơn vạch đường, sơn bể, thùng chứa H2O2, làm giấy bọc chống ẩm...
- Cao su hidro clorua: là cao su thu được do tác dụng của hidro clorua với cao su tự nhiên. Phản ứng cộng xảy ra cũng tuần theo quy tắc Maccopnhicop. Cao su hidroclorua cũng có nhiều ứng dụng, thường dùng để chế sơn, tạo màng chống ẩm.
Ngoài ra, cao su còn tham gia phản ứng với hdiro tạo ra cao su hidro và tác dụng được với lưu huỳnh.
4. Sự lưu hóa cao su
Là sự chế hóa cao su với lưu huỳnh để khắc phục hạn chế của cao su là dính ở nhiệt độ cao, giòn ở nhiệt độ thấp.
Có hai phương pháp lưu hóa cao su:
Lưu hóa nóng: đun nóng cao su với lưu huỳnh ở nhiệt độ khoảng 130-145oC.
Lưu hóa lạnh: chế hóa cao su với dung dịch lưu huỳnh trong CS2. Ở nhiệt độ thường và có thể thay lưu huỳnh bằng S2Cl2.
Khi lưu hóa, một số liên kết pi mở ra, hoặc sự thế ở hidro đính với cacbon bên cạnh nối đôi, tạo thành những cầu nối giữa các mạch polime nhờ các nguyên tố lưu huỳnh, do đó những phân tử rất lớn có cấu trúc mạng lưới không gian được tạo ra:
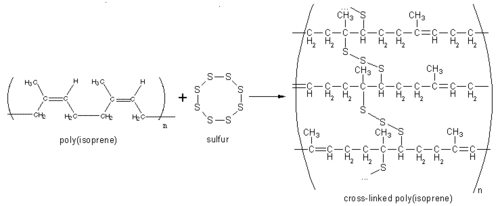
Các phân tử polime cao su trên nhờ có cấu trúc mạng lưới không gian nên tính chất cơ lí hơn hẳn cao su thô: đàn hồi hơn, bền đối với nhiệt, lâu mòn, khó tan trong các dung môi hữu cơ, có khả năng chống thấm khí, chống ẩm tốt hơn.
Thông thường, khối lượng lưu huỳnh trong cao su lưu hóa chiếm khoảng 3- 4% khối lượng cao su thô. Nếu thành phần lưu huỳnh cao hơn (25-40%), sản phẩm tạo thành rất cứng gọi là ebonit dùng làm vật liệu cách điện.
Trong thực tế sản xuất, quá trình lưu hóa coa su thường thực hiện đồng thời với quá trình gia công cao su thành vật phẩm.

.jpg)
.jpg)




.jpg)
.jpg)




















